Eficiencia de cepas bacterianas aisladas del manglar para biorremediar suelos contaminados con petróleo
Beder E. Ramírez Segura, Auberto Hidalgo Mogollón, Alberto Ordinola Zapata, Enedia G. Vieyra Peña, Percy Palacios Moran y Joel Ordinola Madrid
Universidad Nacional de Tumbes, Tumbes Perú.
Recibido: 05/02/2016 - Aceptado: 22/04/2016
Resumen
La adición de bacterias nativas metabolizadoras de hidrocarburos se ha convertido actualmente en una metodología efectiva para biorremediar ambientes contaminados con petróleo. Por tal motivo se aisló y evaluó la capacidad de cinco cepas bacterianas de una zona de manglar del Perú, para biodegradar los hidrocarburos del petróleo. Las bacterias fueron identificadas mediante el gen rRNA 16S y cultivadas en medio mineral Bushnell Hass suplementado con petróleo. Además se realizó un ensayo de bioaumentación durante 28 días en un suelo de manglar que contenía 9,6% de hidrocarburos totales de petróleo (HTP). Las secuencias del gen rRNA 16S de las cepas bacterianas estuvieron 100% relacionadas con Bacillus aryabhattai y Vibrio fluvialis, y 99% con Acinetobacter venetianus, Arthrobacter mysorens y Exiquobacterium profundum. A excepción de la cepa relacionada con B. aryabhattai todas fueron capaces de crecer en el medio mineral suplementado con petróleo. La concentración inicial de HTP en el suelo tratado con el experimento de bioaumentación se redujo entre 77 a 82% con la aplicación de las cepas relacionadas a V. fluvialis, A. venetianus, A. mysorens y E. profundum, los que fueron estadísticamente mayores a la reducción de 68% obtenida con el control negativo. Estos resultados demostraron que en el manglar, existen cepas bacterianas con capacidad para degradar el petróleo y con alto potencial para ser usadas en procesos de biorremediación.
Palabras clave: Bioaumentación, contaminación por petróleo, hidrocarburos totales, bacterias del manglar
Efficiency of bacterial strains isolated from mangroves to bioremediate petroleum-contaminated soil
Summary
The addition of native bacteria metabolizing hydrocarbons has now become an effective methodology for bioremediation of oil-contaminated environments. Therefore it was isolated and evaluated the capacity of five bacterial strains in a mangrove area of Peru, to biodegrade petroleum hydrocarbons. Bacteria were identified by 16S rRNA gene and grown on Bushnell Hass mineral medium supplemented with petroleum. Moreover, a bioaugmentation assay was conducted for 28 days in mangrove soil containing 9,6% of total petroleum hydrocarbons (TPH). The 16S rRNA gene sequences of bacterial strains were 100% related to Bacillus aryabhattai and Vibrio fluvialis and 99% with Acinetobacter venetianus, Arthrobacter mysorens and Exiquobacterium profundum. With the exception of the strain related with B. aerabhattai, the rest of the isolated strains were able to grow in mineral medium supplemented with petroleum. The initial concentration of HPT in the soil treated with the experiment of bioaugmentation was reduced between 77-82% with the application of related strains to V. fluvialis, A. venetianus, A. mysorens and E. profundum, which were statistically greater than removal of 68% obtained with the negative control. These results demonstrate that in the mangroves, there are bacterial strains with ability to degrade petroleum and high potential for use in bioremediation processes.
Keywords: Bioaugmentation, oil pollution, total hydrocarbons, bacteria mangrove
Introducción
A pesar de su importancia económica, la actividad petrolera es una de las actividades humanas que causa grandes impactos sobre el medio ambiente [1]. Diversos eventos de contaminación han ocasionado grandes daños en los ecosistemas marinos frágiles, tanto a nivel mundial [2,3] así como en países de la región [4] y el Perú [5]. Incluso algunos de ellos tales como Sucumbios en la amazonia ecuatoriana [1] y la cuenca del rio Corrientes en Perú [6], aún persisten como pasivos ambientales generando conflictos sociales que afecta la credibilidad de las empresas petroleras [1, 4, 6].
Si bien la atenuación de una cantidad de hidrocarburos en un ecosistema contaminado puede darse de forma natural mediante evaporación, foto-oxidación, emulsión, dispersión y biodegradación [7], en la mayoría de los casos ésta no es suficiente para remediar los sitios contaminados, incluso algunos productos de la foto-oxidación son compuestos más tóxicos que los hidrocarburos originales [8]. Más aún en el caso de los manglares, que debido su alta productividad y su abundante detritus orgánico [9], los hacen un sitio preferencial para la acumulación de hidrocarburos [4], siendo necesario la aplicación de tecnologías que aceleren eficientemente el proceso de remediación.
En este sentido los procesos biológicos, vienen siendo utilizados con éxito para la remediación de sitios contaminados con petróleo ya que su desarrollo puede ser aplicado con un bajo costo económico [10]. Así mismo, diversos estudios han demostrado que entre los procesos biológicos existentes, la bioaumentación con cepas microbianas nativas o aisladas de un mismo ambiente que se pretende biorremediar es un método eficiente y viable para la recuperación de estos ambientes [11-13].
Si bien solo una pequeña parte de la comunidad microbiana puede ser cultivada [14], el aislamiento e identificación de bacterias es importante para entender el rol de estos microorganismos para la metabolización de los hidrocarburos del petróleo [15]. Mediante las técnicas dependientes de cultivo en medios minerales como Bushnell Hass suplementado con diferentes tipos de hidrocarburos [16], se ha aislado y determinado la habilidad de una amplia variedad de géneros bacterianos para degradar diferentes tipos de hidrocarburos en diferentes ambientes como el suelo [11, 17] agua marina [18-20] y manglar [4, 21].
La aplicación de estas bacterias mediante bioaumentación ha logrado reducir entre 45 y 73% la concentración de hidrocarburos totales de petróleo (HTP) en suelos [22, 23]. Entre los géneros aislados con mayor capacidad de biodegradación de hidrocarburos se encuentra Pseudomonas [11, 21, 24], Vibrio [16, 18, 19] Marinobacterium, Marinobacter, Cycloclasticus [25], Rhodococcus [15, 17], Acinetobacter [22, 25], Bacillus [11, 21], Sphingomonas [27, 28], Arthrobacter [29] y Alteromonas [30].
En este sentido el presente trabajo tuvo como objetivo evaluar la capacidad de biodegradación de hidrocarburos del petróleo de cepas bacterianas aisladas a partir de una zona del manglar de Puerto Pizarro, Tumbes.
Materiales y Métodos
Aislamiento microbiológico
El aislamiento de bacterias fue realizado a partir de cinco sub-muestras de 10 gramos de sedimento de una zona de manglar con presencia de hidrocarburos ubicados a 3° 30´ 6,68´´ de latitud sur y 80° 23´ 39,73´´ de longitud oeste, contigua al desembarcadero artesanal de Puerto Pizarro, Tumbes, Perú (Figura 1). Las cinco sub-muestras fueron mezcladas y enrasadas a 100 ml con solución salina (0,85 %) en un matraz estéril a partir del cual se realizó diluciones hasta 10-8. De cada dilución se sembró una alícuota de 100 µl en el medio microbiológico R2A, el cual fue suplementado con 0,25 % de petróleo crudo y se incubó a temperatura ambiente por 24 horas. Cada cepa bacteriana fue sometida a un proceso de purificación mediante siembras continuas en medio R2A. Las cepas bacterianas aisladas fueron codificadas inicialmente de acuerdo a sus características morfológicas (BMRt, FMIt, IPF1, IGF2, TcPF) y conservadasa 4 °C en los medios R2A (medio sólido) y Luria Broth (LB) (marca Oxoid, Reino Unido) hasta su respectiva utilización.
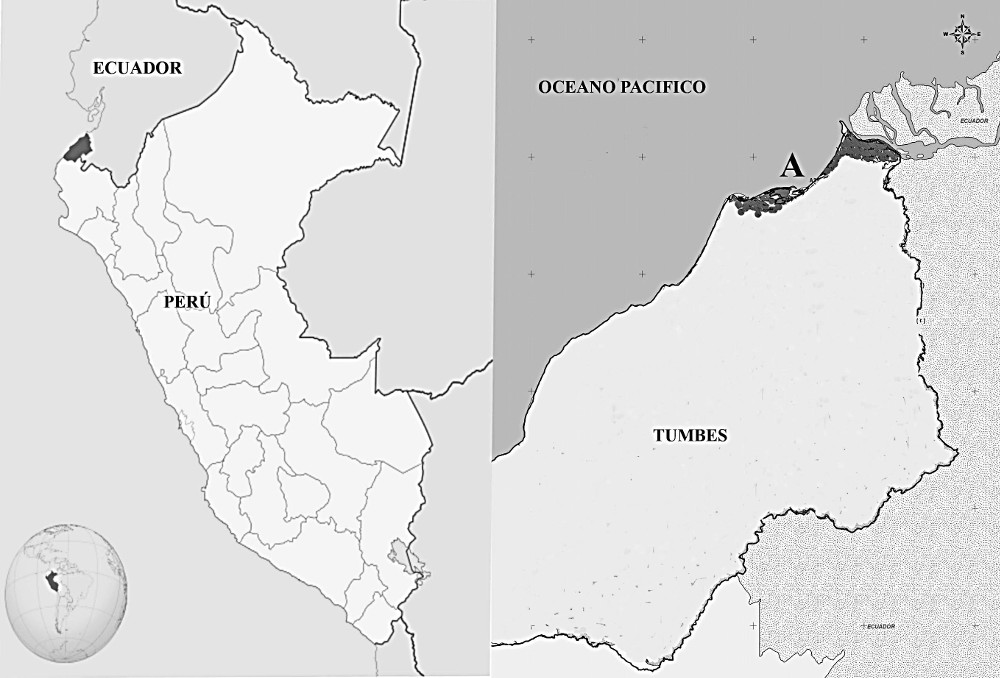
Figura 1: Ubicación geográfica del punto de muestreo A: Zona de manglar del desembarcadero de Puerto Pizarro, Tumbes, Perú.
Identificación molecular de las cepas bacterianas
La extracción de ADN de cada cepa bacteriana, se realizó a partir del 1 ml de cultivo bacteriano incubado por 24 horas y a temperatura ambiente en el medio Luria Broth. Se utilizó el protocolo de extracción de ADN bacteriano con CTAB [31]. La amplificación del gen rRNA 16S se realizó con los iniciadores F8 (5´-AGAGTTTGATYMTGGCTCAG-3´) y R1509 (5´-GNTACCTTGTTACGACTT-3´) propuestos por [32]. Las pruebas de PCR fueron realizadas en un volumen de reacción de 50 µl en un equipo termociclador (marca Biometra, Alemania), utilizando el kit de PCR Taq DNA Polymerase recombinant (marca Thermo Fisher Scientific, EE.UU), de acuerdo a las especificaciones del fabricante. Se consideró una programación de amplificación de 35 ciclos, que consistieron, de 94 °C por 30 segundos en desnaturalización, 57 °C por 30 segundos en hibridación y 72 °C por 45 segundos en polimerización. Los productos obtenidos, fueron migrados electroforéticamente en un gel de agarosa al 2% teñido con bromuro de etidio (0,006 % v/v) (marca Merck, Alemania) y finalmente observados en un transiluminador ultravioleta (marca H.W. Kassel).
La secuenciación fue realizada sobre 15 µl de los productos de la PCR utilizando los iniciadores universales F518 (5´-CCAGCAGCCGCGGTAATACG-3´) y R800 (5´-TACCAGGGTATCTAATCC -3´) en el Laboratorio Macrogen (Maryland, USA). Las secuencias obtenidas fueron editadas y alineadas en el programa informático MEGA 5. La identificación de las cepas bacterianas fue por análisis de las secuencias en la base de datos del National Center for Biotechnology Information (NCBI) mediante la herramienta de análisis Basic Local Alignment Tools (BLAST) (http://www.ncbi.nlm.nih.gov/).
Cultivo microbiológico en medio mineral suplementado con petróleo.
En el laboratorio se desarrolló un cultivo microbiológico en 50 ml del medio mineral Bushnell Hass Broth (marca Microgen, India) suplementado con 500 µl de petróleo crudo (donado por la empresa BPZ Energy, extraído de la plataforma marina de Tumbes) como única fuente de carbono por seis días a temperatura ambiente y con agitación constante de 200 rpm en un equipo Shaker (marca Labnet, EE.UU). El experimento fue realizado por triplicado en 21 matraces considerando las cinco cepas aisladas (BMRt, FMIt, IPF1, IGF2, TcPF) una mezcla de las cinco cepas bacterianas que fue codificada como M5 y un control negativo. Se monitoreó diariamente el crecimiento por observación directa del cambio de coloración en el medio de cultivo.
Ensayo de bioaumentación
Se realizó por triplicado en 21 cajones de madera instalados en un área cercana al manglar de la Facultad de Ingeniería Pesquera y Ciencias del Mar de la Universidad Nacional de Tumbes, Perú. Para esta actividad, se mezcló suelo de manglar con petróleo crudo y se envió 3 muestras de 2 kg solicitada por el Laboratorio Labicer de la Universidad Nacional de Ingeniería en Lima para la determinación de la concentración de hidrocarburos totales mediante cromatógrafo de gases Varian 450-GC. Las muestras tuvieron en promedio 9,6 % de hidrocarburos totales. De esta mezcla se agregó 0,1 m3 en cada cajón y se instaló adicionalmente dos baldes de 16 l que contenían agua del estero en recirculación con la finalidad de mantener siempre húmedo el sustrato (Figura 2). A cada cajón (exceptuando los correspondientes al control) se le agregó cada tres días 50 ml de un cultivo bacteriano de las mismas cepas consideradas en el experimento de laboratorio, durante 28 días. Los cajones correspondientes al control recibieron el mismo volumen del medio de cultivo estéril, durante el mismo periodo de tiempo. Al final del experimento se obtuvo aleatoriamente de cada unidad experimental 5 sub muestras de suelo que fueron mezcladas hasta obtener una muestra final de 2 kg, solicitada por el Laboratorio Labicer de la Universidad Nacional de Ingeniería en Lima para la determinación de la concentración de hidrocarburos totales. La capacidad que tienen diferentes cepas sobre la biodegradación de hidrocarburos fue determinado mediante análisis de varianza, complementado con la prueba de Duncan, todas ellas con α=5%.

Figura 2: Ensayo de biorremediación de suelo de manglar contaminado con petróleo. A) Disposición de los cajones conteniendo el sustrato contaminado con petróleo, se aprecia los baldes para abastecimiento y recojo del agua, B) Vista del sustrato húmedo contenido en uno de los cajones.
Resultados
Aislamiento de bacterias
Se contabilizó en total 8,0x105 de UFC/g de suelo. De este grupo, las cinco cepas de bacterias aisladas (Tabla 1), tuvieron una similitud en sus secuencias del gen rRNA 16S de 100% con Bacillus aryabhattai (KC934850.1), y Vibrio fluvialis (JQ650110.1) y de 99% con Acinetobacter venetianus (AB859738.1), Arthrobacter mysorens (AJ639831.1) y Exiquobacterium profundum (AY745848.1).
| Código de cepa | Color de colonia | Forma de colonia | Tamaño de colonia | Identidad filogenética |
| BMRt | Blanca | Redonda | Mediana | Bacillus aryabhattai |
| FMIt | Fluorescente | Irregular | Mediana | Exiquobacterium profundum |
| IPF1 | Fluorescente | Irregular | Pequeña | Acinetobacter venetianus |
| IGF2 | Fluorescente | Irregular | Grande | Vibrio fluvialis |
| TcPF | Fluorescente | Concéntrica | Pequeña | Arthrobacter mysorens |
Tabla 1: Morfología de las colonias e identidad filogenética de las cepas bacterianas aisladas de sedimento de una zona de manglar.
Cultivo microbiológico en medio mineral suplementado con petróleo.
Tanto el tratamiento que contuvo la mezcla de las cinco cepas de bacterias estudiadas (M5) así como los tratamientos con las cepas individuales relacionadas con Vibrio fluvialis (IGF2),Acinetobacter venetianus (IPF1),Arthrobacter mysorens (TcPF) y Exiquobacterium profundum (FMIt), tuvieron la capacidad de crecer en el medio mineral suplementado con petróleo. Mientras que la cepa relacionada a Bacillus aryabhattai (BMRt) así como el control negativo no mostraron crecimiento manteniéndose el color del medio microbiológico transparente durante el periodo de ensayo.
Ensayo de bioaumentación
El suelo de manglar mezclado con petróleo tuvo una concentración promedio inicial de HTP de 9,6%. Después de los 28 días que duró el ensayo de bioaumentación los tratamientos con las cepas IGF2 (Vibrio fluvialis) TcPF (Arthrobacter mysorens), IPF1 (Acinetobacter venetianus) y FMIt (Exiquobacterium profundum) produjeron respectivamente una disminución de 82 %, 81 %, 77 % y 77 % de la concentración inicial de los HTP (Tabla 2). Estos valores fueron estadísticamente mayores que el control negativo (C-), el cual que alcanzó un 68 % de remoción de los HTP. Así mismo al final del proceso, las características organolépticas de color y olor del suelo impactadas por la contaminación de petróleo mejoraron hasta tener las características cercanas a un suelo normal.
| Tratamientos | Promedio ± desv. estándar | Remoción de HT (%) |
|---|---|---|
| Control negativo | 3,038±0,142a* | 68 |
| BMRt | 2,523±0,126ab | 74 |
| TcPF | 2,178±0,313bc | 77 |
| IPF1 | 2,171±0,612bc | 77 |
| FMIt | 1,833±0,421bc | 81 |
| M5 | 1,743±0,064c | 82 |
| IGF2 | 1,713±0,107c | 82 |
Tabla 2: Concentración porcentual de hidrocarburos totales (HTP) en el suelo a los 28 días de iniciado el experimento según tratamiento de suelos de manglares de Tumbes, Perú. * Letras iguales representan valores estadísticamente similares de acuerdo a la prueba de Duncan con α = 0,05.
Discusión
El presente estudio determinó la capacidad de las cepas bacterianas IGF2 (Vibrio fluvialis), IPF1 (Acinetobacter venetianus), FMIt (Exiquobacterium profundum) y TcPF (Arthrobacter mysorens) aisladas del manglar, para crecer en un medio microbiológico mineral teniendo al petróleo como única fuente carbono. Estas cepas redujeron significativamente la concentración de HTP mediante bioaumentación en un suelo contaminado con petróleo (Tabla 2).
Los géneros que están relacionadas con las cepas bacterianas encontradas en presente estudio (Vibrio, Acinetobacter y Arthrobacter), también han sido identificados en trabajos previos como bacterias con capacidad de biodegradación de hidrocarburos, como por ejemplo el reporte de Acinetobacter para degradar hidrocarburos totales [22, 33], degradadoras de alcanos [26] y de alifáticos [17]. El género Arthrobacter ha sido relacionado con la degradación de los hidrocarburos aromáticos policíclicos como el flureno [29], así como de hidrocarburos aromáticos más complejos como el 4-nitrofenol [34]. En el caso del género Vibrio, se han aislado cepas marinas de Vibrio parahaemolyticus y Vibrio fluvialis, con capacidad para degradar fenantreno [35], Vibrio splendidus con capacidad para degradar naftaleno y fenantreno [18] y Vibrio cyclotrophicus con capacidad para degradar a los PAH [19]. Generalmente estas bacterias han sido aisladas de ambientes diferentes al manglar por lo que los resultados encontrados en éste estudio además de contrastar la capacidad de estas bacterias para biodegradar los HTP también amplían la distribución ecológica de este tipo de bacterias.
En el ensayo de bioaumentación desarrollado en la presente investigación se observó, que la cepa que produjo la mayor disminución en la concentración promedio de HTP fue IGF2 (Vibrio fluvialis) que disminuyó los HTP desde 9,6 % hasta 1,7 ± 0,1 %, representando un 82 % de remoción total de los HTP. El porcentaje de remoción de HTP durante este trabajo fue mayor a lo obtenidos por Menezes y colaboradores [22] y Przystaś y colaboradores [23] los que de forma independiente lograron una remoción de alrededor de 73% utilizando consorcios bacterianos. La capacidad de especies del género Vibrio para la degradación de hidrocarburos también ha sido demostrado por Geiselbrecht y colaboradores [18], quienes encontraron que Vibrio spp. tuvo un crecimiento mayor sobre un medio con hidrocarburos que otras cepas de Cycloclasticus spp. Esto muestra que Vibrio es capaz de mantener un crecimiento acelerado, probablemente debido a un aprovechamiento más eficiente de los hidrocarburos totales lo que explicaría porque fue capaz de reducir en mayor grado los niveles de HTP en el presente proyecto.
La disminución de HTP observado en el control negativo, se podría deber a la acción de la microbiota del suelo [2, 33] así como también a factores físicos como la luz solar y la temperatura ambiental, los que pueden contribuir con la evaporación, fotoxidación, emulsión, dispersión y biodegradación de los hidrocarburos [4, 7]. Esta acción natural se vio reforzada con la adición de las cepas bacterianas aisladas ya que claramente se pudo observar (Tabla 2) que todos los tratamientos tuvieron un rendimiento mayor al control negativo, sobre todo por las cepas IGF2 (Vibrio fluvialis), FMIt (Exiquobacterium profundum), IPF1 (Acinetobacter venetianus) y TcPF (Arthrobacter mysorens). El crecimiento en el medio mineral Bushnell Haas suplementando con petróleo como única fuente de carbono, mostrado por las cepas IGF2 (Vibrio fluvialis), IPF1 (Acinetobacter venetianus) y TcPF (Arthrobacter mysorens) es también un indicador de la capacidad de estas bacterias para degradar los hidrocarburos del petróleo [12, 36].
Debido a la capacidad para degradar los hidrocarburos del petróleo, las cepas IGF2 (Vibrio fluvialis), IPF1 (Acinetobacter venetianus), FMIt (Exiquobacterium profundum) y TcPF (Arthrobacter mysorens) aisladas del manglar pueden ser utilizadas para numerosas aplicaciones biotecnológicas tanto en el área ambiental como industrial [12]. Además el uso de estas cepas mediante métodos dependientes del cultivo permitiría examinar en detalle las rutas degradativas y evaluar sus estrategias de subsistencia bajo condiciones altamente desfavorables que ocurren en un derrame.
La presencia de bacterias con capacidad para degradar los hidrocarburos del petróleo, permitiría inferir que el área de suelo estudiado tendría cierta capacidad natural para enfrentarse a perturbaciones externas relacionadas con la contaminación por petróleo [2, 33]. La que se vería incrementado con la aplicación de la técnica de bioaumentación mediante la inoculación de las cepas aisladas que presentaron mayor actividad durante este trabajo de investigación. Dado que se ha demostrado [12, 13] que el uso de bacterias nativas hacen que la bioaumentación sea mucho más eficiente para acelerar la recuperación de estos ambientes contaminados.
Conclusiones
1. Se determinó mediante cultivo en medio mineral suplementado con petróleo, que las cepas bacterianas IGF2 (Vibrio fluvialis), IPF1 (Acinetobacter venetianus), FMIt (Exiquobacterium profundum) y TcPF (Arthrobacter mysorens) tienen la capacidad para degradar y utilizar los hidrocarburos del petróleo como fuente de carbono.
2. Se determinó que el uso de las cepas IGF2 (Vibrio fluvialis), IPF1 (Acinetobacter venetianus), FMIt (Exiquobacterium profundum) y TcPF (Arthrobacter mysorens) mediante el método de bioaumentación mejora el proceso de biorremediación de un suelo de manglar contaminado con petróleo.
3. El método de bioaumentación se presenta como una buena alternativa para recuperar el suelo del manglar ante una posible contaminación por el derrame de petróleo, generando un beneficio ambiental.
Agradecimientos
A la oficina de investigación de la Universidad Nacional de Tumbes por el financiamiento económico del presente proyecto. Al Ing. Raúl Coveñas de la empresa BPZ energy por la donación de petróleo crudo. Al Dr. Ingo Werhrtmann por su colaboración en la revisión del presente artículo
Referencias
1. Roa T. (2011). La triste historia ambiental del extractivismo petrolero. Petropress 25(1): 4-10
2. Swannell R, Lee K, y McDonagh M. (1996). Field evaluations of marine oil spill bioremediation. Microbiological Review 60(2): 342-365.
3. Barth H. (2002). The 1991 Gulf War Oil Spill: Its ecological effects and recovery rates of intertidal ecosystems at the Saudi Arabian Gulf coast - results of a 10-year monitoring period. Regensburg, Alemania: Universidad de Regensburg.
4. Olguin J, Hernández M, y Sánchez-Galván G. (2007). Contaminación de manglares por hidrocarburos y estrategias de biorremediación, fitorremediación y restauración. Revista Internacional Contaminación Ambiental 23 (3): 139-154
5. Austermühle S. (2010). Historia de derrames de petróleo en el Perú. Lima, Perú: ONG Grupo Mundo Azul.
6. Feconaco y Shinai. (2011). Impactos petroleros en territorios indígenas: Experiencias del programa de vigilancia territorial del río Corrientes. Iquitos Perú: 12-14
7. Brakstad O, y Bonaunet K. (2006). Biodegradation of petroleum hydrocarbons in seawater at low temperatures (0–5 °C) and bacterial communities associated with degradation. Biodegradation 17(1): 71-82.
8. Lee R. (2003). Photo-oxidation and photo-toxicity of crude and refined oils. Spill Science & Technology Bulletin 8(1): 157-162.
9. Lewis R. (2005). Ecological engineering for successful management and restoration of mangrove forests. Ecological Engineering 24(1): 403-418.
10. Garzón C, y Barragán B. (2008). Inmovilización microbiana: técnicas y usos en el tratamiento de residuos tóxicos. Revistas Sistemas Ambientales 2(1):23-34
11. Das K, y Mukherjee A. (2006). Crude petroleum-oil biodegradation efficiency of Bacillus subtilis and Pseudomonas aeruginosa strains isolated from a petroleum-oil contaminated soil from North-East India. Bioresource Technology 98(7): 1339-45.
12. Benavides J, Quinteros G, Guevara A, Jaimes D, Gutiérrez S, y Miranda J.(2006). Biorremediación de suelos contaminados con hidrocarburos derivados del petróleo. Nova Publicación Científica 4(5): 1-116
13. Raiger L, y López R. (2009). Los biosurfactantes y la industria petrolera. Revista Química Viva 3(8): 146-161.
14. Amann R, Ludwig W, y Schleifer K. (1995). Phylogenetic identification and in situ detection of individual microbial cells without cultivation. American Society for Microbiology 59(1): 143–169.
15. Correa F, Colombo L, y Zachia M. (1993). Production of biosurfactant by hydrocarbon degrading Rhodococcus ruber and Rhodococcus erythropolis. Revista de Microbiología 30(3): 231-236.
16. Hernandez A, Martínez J, Cruz y Ramos R. (2002). Capacidad biodegradativa de cepas de Vibrio sobre una mezcla de hidrocarburos. Foresta Veracruzana 4(2): 29-38.
17. Acuña A, Pucci G, Morales M, y Pucci O. (2010). Biodegradación de petróleo y sus derivados por la comunidad bacteriana en un suelo de la Patagonia Argentina. Revista de la Sociedad Venezolana de Microbiología 30(1): 29-36.
18. Geiselbrecht A, Herwig R, Deming J, y Staley J.(1996). Enumeration and phylogenetic analysis of polycyclic aromatic hydrocarbon-degrading marine bacteria from puget sound sediments. Applied and Environmental Microbiology 62(9): 3344-3349
19. Hedlund P, y Staley J. (2001). Vibrio cyclotrophicus sp. nov., a polycyclic aromatic hydrocarbon (PAH)-degrading marine bacterium. International Journal of Systematic and Evolutionary Microbiology 51(1): 61–66
20. Harwati T, Kasai Y, Kodama Y, Susilanincsih D, y Watanabe K. (2007). Characterization of diverse hydrocarbon degrading bacteria isolated from Indonesian seawater. Microbes Environments 22(4): 412-415.
21. Anayo F, Ibiene A, y Okerentugba PO. (2013). Bioremediation of petroleum hydrocarbon polluted mangrove swamps using nutrient formulas produced from water hyacint (Eicchornia crassipes). American Journal of Environmetal Science 9(4): 348-366
22. Menezes F, Anastácio F, Okeke B, y Frankenberger T.(2003). Biorremediation of soil contaminated by diesel oil. Brazilian Journal of Microbiology34(1):65-68
23. Przystaś W, Pasadakis N, y Kalogerakis N. (2010). Bioremediation of petroleum contaminated sands with bacteria cultures. Architecture Civil Engineering Environment 3(1): 105-114
24. Whyte L, Bourbonniere G, y Greer C. (1997). Biodegradation of petroleum hydrocarbons by psychrotropic Pseudomonas strains possessing both the alkane (alk) and naphthalene (nah) catabolic pathways. Applied and Environmental Microbiology 63(1): 3719–3723.
25. Fragoso H, Carvalho J, Lima F, Lopes A, Tiedje J, Dirk J, Soares A, y Silva R. (2011). Mangrove bacterial diversity and the impact of oil contamination revealed by pyrosequencing: Bacterial proxies for oil pollution. Plos One 6(3): e16943
26. Díaz M, Grigson S, y Burgess J. (2002). Uso de un consorcio bacteriano extremo-halotolerante para la biodegradación de crudo en ambientes salinos. Revista Colombiana de Biotecnología 4(1): 36-42.
27. Berardesco G, Dyhrman S, Gallagher E, y Shiaris M. P. (1998). Spatial and temporal variation of phenanthrene-degrading bacteria in intertidal sediments. Applied and Environmental Microbiology 64(1): 2560-2565.
28. Sabaté, J, Grifoll M, Viñas M, y Solanas A. (1999). Isolation and characterization of 2-methyl-phenanthrene utilizing bacterium: identification of ring cleavage metabolites. Applied and Environmental Microbiology 52(1): 704-712.
29. Grifoll M, Casellas M, Bayona J, y Solanas A. (1992). Isolation and characterization of a fluorene-degrading bacterium: identification of ring oxidation and ring fission products. Applied and Environmental Microbiology 58(9): 2910-2917.
30. Jin H, Kim J, Lee H, Madsen E y Jeaon C. (2012). Alteromonas as a key agent of polycyclic aromatic hydrocarbon biodegradation in crude oil contaminated coastal sediment. Environmental Science Technology 46(14): 7731-7740
31. Wilson K. (1997). Current protocols in molecular biology. Townsville, Australia: Australian Institute of Marine Science.
32. Peu P, Brugere H, Pourcher A, Kerouredan M, Godon J, Delgenes J, y Dabert P. (2006). Dynamics of a pig slurry microbial community during anaerobic storage and management. Applied and Environmental Microbiology 72(5): 3578-3585.
33. Gómez, A. (2011). Evaluación de la actividad y la diversidad bacteriana con potencial biorremediador asociada a diferentes profundidades en el suelo del morro de Moravia mediante análisis de secuencias del gen 16s rDNA. Tesis de maestría en biotecnología, Universidad Nacional de Colombia.
34. Jain R, Dreisbach J, y Spain C. (1994). Biodegradation of p-nitrofenol via 1,2,4-benzenetriol by an Arthrobacter sp. Applied and Environmental Microbiology 60(8): 3030
35. West P, Okpokwasili G, Brayton P, Grimes D, y Colwell R.(1984). Numerical taxonomy of phenanthrene degrading bacteria isolated from the Chesapeake Bay. Applied and Environmental Microbiology 48(1): 988-993.
36. Rivera M, Ferrera R, Volke V, Rodríguez R y Linares L.(2000). Adaptación y selección de microorganismos autóctonos en medios de cultivos enriquecidos con petróleo crudo. Terra 20(1): 423-434.
|
Revista QuímicaViva Número 1, año 15, Agosto 2016 quimicaviva@qb.fcen.uba.ar |