La importancia cualitativa de los números en la enseñanza de la Biología. Aprendizaje sustentable del potencial de acción
Nazira Píriz Giménez1,2, Jerónimo Tucci 1,3 y María Noel López 2,4,5
1 Instituto de Profesores “Artigas”, Consejo de Formación en Educación; 2 Profesorado Semipresencial, Consejo de Formación en Educación; 3 Liceo N°25, Consejo de Educación Secundaria; 4 Centro Regional de Profesores del Centro, Consejo de Formación en Educación; 5 Escuela Integral de Montevideo. Montevideo. Uruguay
Recibido: 9/10/2018 - Aceptado: 19/10/2018
Resumen
La enseñanza de la membrana celular, como vínculo entre los medios intracelular y extracelular, y en particular los mecanismos de transporte de solutos, constituye un contenido esencial dentro del estudio de la Biología celular. Una de las dificultades que desde la enseñanza de la Biofísica hemos tenido históricamente ha sido la función de la bomba de sodio y potasio. Especialmente, la adjudicación a dicho transportador, de la responsabilidad de la fase de repolarización en el potencial de acción. En un segundo lugar y de menor gravedad, suele no relacionarse a dicho transportador con el mantenimiento del volumen en células animales. El primero de dichos obstáculos constituye un problema relevante que hemos analizado, encontrando que el mismo se origina en la creencia de que durante el potencial de acción, las concentraciones de sodio y potasio se modifican sustancialmente en las células. Para atender esta problemática hemos elegido estrategias diferentes en cursos de grado y de formación continua, en tanto que aún persiste en textos o páginas web. La estrategia didáctica utilizada radica en generar conceptos de sostén correctos para lograr un aprendizaje sustentable. En este trabajo describimos nuestra propuesta y explicamos su fundamentación.
Palabras clave: bomba de sodio y potasio; potencial de acción; enseñanza de la Biología; concepto sostén; aprendizaje sustentable.
Summary
The teaching of the cell membrane, as a link between the intracellular and extracellular media, and in particular the mechanisms of solute transport, constitutes an essential content in the study of cellular biology. One of the difficulties that the teaching of biophysics has had historically has been the function of the sodium and potassium pump. On one hand, it is a mistake to consider that this transporter is responsible for the repolarization phase in the action potential. In a second place, other problem is not to relate this transporter with the maintenance of volume in animal cells. The first obstacle would originate the belief that the concentrations of sodium and potassium are substantially modified in the cells during the action potential. To address these problems we have chosen different didactic strategies to be implemented in courses, although they still persist in texts or web pages. The used didactic strategy has considered construct proper support concepts to achieve sustainable learning. In this paper we describe our proposal and explain its rationale.
Keywords: sodium/potassium pump; action potential; Biology teaching; support concept; Sustainable Learning
Introducción
Las membranas biológicas delimitan y vinculan compartimentos con diferente composición manteniendo así el “orden” característico de los seres vivos. Dicha vinculación incluye el pasaje de solutos a través de las membranas celulares y de organelos, procesos que son de gran relevancia para el mantenimiento de funciones vitales.
El pasaje de solutos a través de las membranas biológicas se da o bien a través de la bicapa lipídica (en el caso de solutos liposolubles), o bien a través de proteínas transportadoras de diverso tipo (en el caso de solutos hidrosolubles, tales como iones inorgánicos pequeños).
Los iones inorgánicos de mayor relevancia biológica son: Na+, K+, Ca++ y Cl-. Dentro de las proteínas transportadoras que hacen posible su pasaje a través de membranas, se encuentran: a.- los canales iónicos (permiten únicamente el transporte pasivo de iones, es decir que utilizan la energía provista por el gradiente electroquímico del ión1) y lo realizan con alta especificidad (de manera que no permiten el pasaje de cualquier ión, sino únicamente aquél del que toman su nombre); b.- las bombas (permiten el transporte activo de iones y por ende en contra de gradiente electroquímico; en las que casi siempre la energía es provista por la hidrólisis del ATP); c.- los transportes acoplados (hacen posible el transporte activo de un soluto por una proteína que permite el pasaje pasivo simultáneo de un segundo soluto, sin consumo directo de ATP). Dichos mecanismos difieren también considerablemente en la rapidez con la que hacen posible el pasaje de iones a su través (Fig. 1).
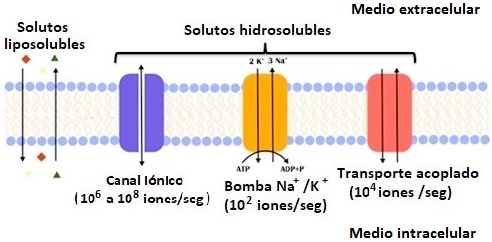
Figura 1: Representaciones gráficas sobre mecanismos de transporte de solutos a través de membranas biológicas.
Con respecto a las bombas, una de las más conocidas y presente en las células animales, es la “bomba de sodio y potasio”, que saca 3 iones sodio al medio extracelular e ingresa 2 iones potasio al medio intracelular, por cada molécula de ATP que hidroliza (Fig. 1). Hay acuerdo en el ámbito científico en que la relevancia fisiológica de este mecanismo de transporte radica en el mantenimiento del equilibrio osmótico y el volumen en células animales [1,2]. Es decir, que permite en condiciones fisiológicas el mantenimiento constante del volumen celular. Sin embargo, la bomba de sodio y potasio tiene muy escasa participación en el potencial de membrana de reposo (menos del 10% de su valor), y ninguna participación en respuestas eléctricas de las membranas celulares2.
Por otra parte, los canales iónicos adoptan en condiciones fisiológicas, diversas configuraciones denominadas “estados”. A modo de ejemplo, los canales de sodio pueden estar abiertos, inactivos o cerrados, en tanto que los de potasio pueden estar únicamente abiertos o cerrados, tal como se representa gráficamente en la figura 2. Cabe considerar que el único estado que permite el pasaje de iones a su través es el estado “abierto”, no así los estados “cerrado” o “inactivo”. Una diferencia relevante entre estos dos últimos, radica en que mientras el canal cerrado puede abrirse, el canal inactivo debe cerrarse en primer lugar para luego estar en condiciones de abrirse.
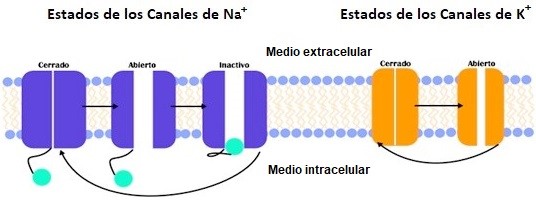
Figura 2: Representación gráfica de los estados de los canales de sodio y potasio. Con flechas se indica la secuencia de sus cambios.
Respuestas eléctricas de la membrana celular: el caso del potencial de acción neuronal
El transporte de iones a través de las membranas celulares constituye un pasaje de cargas eléctricas por unidad de tiempo, por lo que puede medirse como una “corriente eléctrica”. Dicha corriente modifica el valor del potencial de membrana (Vm), definido como la diferencia entre los voltajes intracelular (Vi) y extracelular (Ve): Vm = Vi – Ve. Todas las células vivas tienen un valor de Vm que cuando permanece estable se denomina “potencial de membrana de reposo”. Este queda determinado por la diferente distribución de iones a ambos lados de la membrana celular y especialmente por la alta permeabilidad al potasio, siendo esta última responsable de la cercanía entre el valor de Vm y el valor del potencial de equilibrio electroquímico de dicho ión. Cuando el valor de Vm “sale del reposo”, se produce una “respuesta eléctrica” de la membrana celular. Una de ellas es el potencial de acción, denominado así porque se propaga en forma “activa”, lo que significa que se autorregenera. Es decir, la zona de la membrana celular en la que tiene lugar un potencial de acción, modifica las zonas vecinas despolarizándolas y determinando que en ellas se alcance un umbral tal que dispare también un potencial de acción, y, así, sucesivamente. El potencial de acción más conocido en la enseñanza de la Biología, es el que se produce en neuronas y al que suele denominársele “impulso nervioso”.
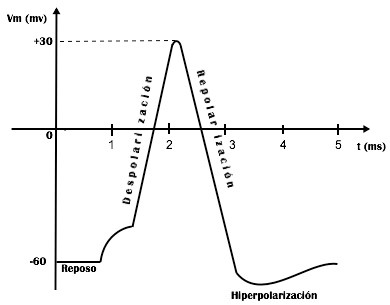
Figura 3: Potencial de acción neuronal “típico” y sus fases.
Durante dicha respuesta, el valor de Vm cambia desde un valor negativo “de reposo” (-60 mV en la Fig. 3), hacia valores más positivos durante la fase de despolarización, alcanzando un pico en los 30mV aproximadamente, y luego volviendo hacia el valor de reposo (fase de repolarización). En algunas neuronas la fase de repolarización es seguida de una reducción a valores de Vm por debajo del valor de reposo que se denomina hiperpolarización. Este potencial de acción es generado por corrientes de Na+ y K+ a través de canales específicos. La corriente entrante de Na+ se activa en un Vm dado “umbral” y dispara la fase de despolarización. Dicho “disparo” es consecuencia de una retroalimentación positiva en la que la despolarización abre canales y el ingreso de Na+ produce mayor despolarización y apertura de canales. En menos de 0,5 mseg, la conductancia3 (permeabilidad) al ión sodio pasa de un valor casi nulo (en el reposo), a 30 mmho/cm2 en el pico del potencial de acción . También en el umbral pero con una cinética más lenta, se abren canales de K+ que permiten una corriente saliente de dicha especie iónica. La inactivación de los canales de Na+, en conjunto con el aumento en la corriente de K+, determinan el cese de la despolarización y el inicio de la repolarización. El mantenimiento de la corriente saliente de potasio origina la fase de hiperpolarización (el Vm se hace más negativo que el valor de reposo) en ciertas neuronas [1, 2, 3, 4, 5].
El potencial de membrana es un fenómeno local (se da en las inmediaciones de la membrana celular) y los flujos iónicos (sumamente rápidos) que lo determinan, no alteran las concentraciones iónicas intra y extracelulares 5.
Enfatizamos aquí, por lo tanto, que los mecanismos moleculares que determinan el potencial de acción, no incluyen a la bomba de sodio y potasio.
La bomba de sodio y potasio:
Antes de que se descubriera la bomba de sodio y potasio [6], ya se infería algún mecanismo activo responsable del mantenimiento de los gradientes electroquímicos de sodio y potasio en las células vivas. La bomba de sodio y potasio transporta en contra de gradiente electroquímico (y por ende en forma activa), 3 iones Na+ y 2 iones K+, por cada molécula de ATP que hidroliza, manteniendo los gradientes electroquímicos de ambos iones. Sin dudas, el mantenimiento de los gradientes electroquímicos resulta esencial en la señalización celular eléctrica, ya que la existencia de dichos gradientes determina el pasaje pasivo de iones (que tiende a disminuir cada gradiente electroquímico) durante las respuestas eléctricas como el potencial de acción.
Es conocida la distribución “universal” de la bomba de sodio y potasio en la enorme mayoría de las células animales, incluso en aquellas que no son excitables (es decir que no disparan potenciales de acción). Cabe considerar también, que otras células, no animales también son excitables y sin embargo no cuentan en sus membranas con bombas de sodio y potasio (organismos unicelulares como Paramecium, células de plantas que responden con el movimiento de sus hojas como Mimosa púdica, entre otros). Puede inferirse entonces que este transportador no es el único responsable del mantenimiento de gradientes electroquímicos en las células vivas, que hacen posible la señalización eléctrica.
En las células animales la actividad de la bomba de sodio y potasio no sólo mantiene los gradientes de ambos iones, sino que dado que por cada molécula de ATP que hidroliza, saca 3 partículas e ingresa 2, contribuye a la disminución de la osmolaridad intracelular, y, por lo tanto, al mantenimiento del volumen celular [1,2].
La actividad de la bomba de sodio y potasio se mantiene inalterada en tanto disponga de ATP, pero es independiente del valor de Vm y por ende de que la membrana se encuentre o no en reposo.
El mito de la bomba de sodio y potasio
En el imaginario de docentes y estudiantes de Ciencias, es frecuente detectar que la bomba de sodio y potasio es considerada como la responsable de la repolarización del potencial de acción. Este concepto a modo de ejemplo en la webgrafía). La bomba de sodio y potasio permite – erróneo coincide con información provista en diferentes fuentes, especialmente internet (se citan páginas como se mencionó previamente– que por cada molécula de ATP que hidroliza, salgan tres iones Na+ de la célula y entren dos K+ (Fig.1), dando en balance una corriente catiónica saliente que hace más negativo al potencial de membrana. A esto se debe el carácter electrogénico de la bomba de sodio y potasio. No obstante, dicho carácter contribuye escasamente al valor de Vm (menos del 10% del potencial de reposo) [1,2,4,5]. Quienes atribuyen la responsabilidad de la bomba de Na+ y K+ a la repolarización del potencial de acción, consideran erróneamente que éste sería el mecanismo compensatorio de la fase de despolarización en la que ocurre la entrada masiva de iones Na+. Pero esta hipótesis es errónea [2,3] pues la bomba de sodio y potasio está distribuida en toda la membrana celular, y no es responsable de reestablecer las concentraciones iónicas que acompañarían la vuelta del Vm al valor de reposo, ya que tales cambios transitorios en las concentraciones intra y extracelulares son mínimos y microlocalizados [7].
El mito de la implicancia de la bomba de Na+/K+ durante el proceso de potencial de acción podría provenir de una cierta lógica de compensación de procesos, mediante la sentencia errónea que sostiene que “las concentraciones iónicas se modificarían drásticamente durante el potencial de acción, y la bomba de sodio y potasio resolvería dicho cambio durante la fase de repolarización”; y, también, encontraría refuerzos visuales en imágenes o representaciones gráficas erróneas, como las que se muestran en la Figura 4.
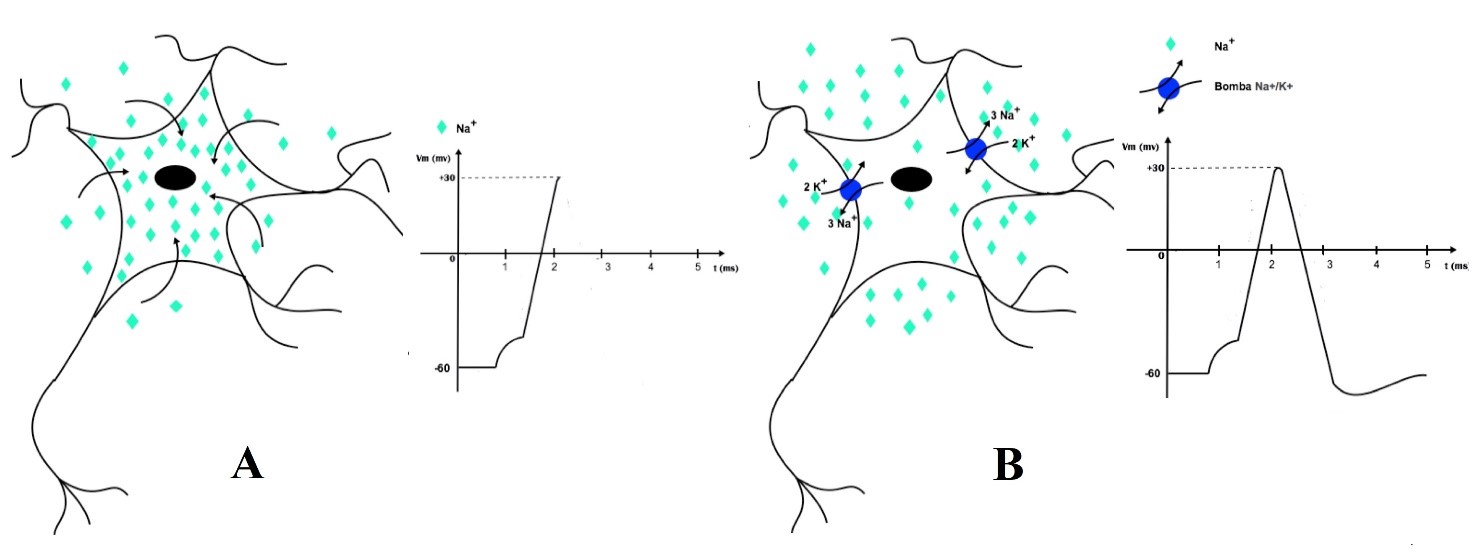
Figura 4: Representaciones gráficas erróneas asociadas al mito de la bomba de sodio y potasio
La Figura 4 remite claramente a los dos errores conceptuales que conducirían a un aprendizaje erróneo del potencial de acción. A: Concepto erróneo respecto a un incremento en la concentración de Na+ intracelular, que ocurriría durante la despolarización. B: Concepto erróneo respecto a cómo la bomba de Na+/K+ revertiría el incremento en la concentración de Na+ intracelular, durante la fase de repolarización. Ilustran estos conceptos erróneos las siguientes informaciones tomadas de internet:
(tomado de http://webspace.ship.edu/cgboer/genesp/potencial_accion.html).
(tomado de http://recursos.cnice.mec.es/biosfera/alumno/1bachillerato/animal/contenidos16.htm).
Conceptos sostén para un aprendizaje apropiado
Analizando esta situación desde la perspectiva del Modelo de Aprendizaje Cognitivo Conciente Sustentable (MACCS) [8,9] es posible plantear que un aprendizaje erróneo tendría su origen en conceptos inclusores equívocos tales como:
a) Que la actividad de la bomba de sodio y potasio revertiría la despolarización provocada por corrientes a través de canales iónicos, con una eficacia similar, en un intervalo de tiempo similar. Este concepto implicaría una rapidez semejante para el pasaje de iones a través de mecanismos de transporte, sin considerar que el flujo iónico a través de proteínas canal es entre 104 y 106 veces mayor que el flujo a través de bombas.
b) Que la actividad de la bomba de sodio y potasio aumentaría durante la fase de repolarización, es decir que al final de la despolarización se incrementaría su función, lo que implicaría una actividad modulada por el potencial de membrana, no conocida hasta el momento.
Siguiendo las sugerencias del MACCS, nos propusimos abordar esta problemática mediante la realización de diversas actividades que contemplaran los conceptos sostén definidos como relevantes, y permitieran derribar el “mito de la bomba de sodio y potasio”, contribuyendo a un aprendizaje sustentable del potencial de acción. Esta propuesta fue desarrollada en un curso de formación continua para docentes, en el Instituto de Profesores “Artigas” de Montevideo [9] A continuación, relatamos las ideas centrales de la propuesta, así como los principales resultados y reflexiones.
En la propuesta desarrollada definimos un concepto sostén central y conceptos sostén complementarios.
El primero de ellos consiste en que la rapidez con que pasan los iones a través de las membranas celulares permite que un número escaso de iones sea suficiente para determinar un cambio en el potencial de membrana biológicamente sustantivo.
Dentro de los conceptos sostén complementarios identificamos:
- Durante un potencial de acción nervioso es muy escasa la cantidad de carga y por ende la cantidad de iones transportada a través de la membrana celular, y dadas las concentraciones iónicas habituales, éstas no son modificadas por dichos flujos;
- El pasaje de iones a través de canales es entre 104 y 106 veces más rápido que el pasaje de iones a través de bombas;
- Las duraciones de las fases de despolarización y repolarización del potencial de acción son muy similares, por lo que no es posible que si la primera queda determinada por el pasaje de iones a través de canales, la segunda quedara determinada por un mecanismo entre 104 y 106 veces más lento;
- Una hipotética actividad de la bomba de sodio y potasio durante la fase de repolarización que pudiera contrarrestar lo ocurrido durante la despolarización, implicaría que dicha bomba aumentara su actividad en la segunda fase del potencial de acción, y posiblemente que se activara por despolarización. En cambio, la bomba de sodio y potasio mantiene una actividad constante, e independiente del valor de Vm;
Cuando los números importan en la enseñanza de la Biología
Dentro de las actividades desarrolladas para el logro de los conceptos sostén relatados, las que mostraron mayor impacto en la población destinataria fueron las que permitieron comparar la rapidez de la actividad de la bomba de sodio y potasio, con la de los canales iónicos. Llevar esta comparación a ejemplos cotidianos permitió dimensionar con claridad dos conceptos:
- Que no es posible que durante un potencial de acción las concentraciones iónicas cambien sustancialmente;
- Que aún en el caso de que esos cambios se dieran, es inviable que la bomba de sodio y potasio revierta los efectos en el valor de Vm determinados por el pasaje de iones a través de canales, en un intervalo de tiempo similar.
A modo ilustrativo, lo descrito es comparable a la diferencia de velocidad entre una sonda espacial y una persona que trota. Se estima que la sonda Juno alcanzó al pasar por Júpiter velocidades superiores a los 240.000 Km/h. Si consideramos que una persona puede trotar a 6 Km/h, la sonda supera en 40.000 veces la rapidez de la persona. Si a la sonda Juno le llevó 5 años viajar desde la Tierra a Júpiter, ¿cuánto le llevaría a una persona trotando? Dejando de lado aspectos como el tiempo de vida de las personas y la imposibilidad de recorrer esa distancia en el espacio, la comparación permite dimensionar las diferencias. Actividades formuladas en base a estas ideas y representadas en la Figura 5, causaron sorpresa en los destinatarios del curso descrito y permitieron comprender con claridad, los conceptos sostén elegidos.
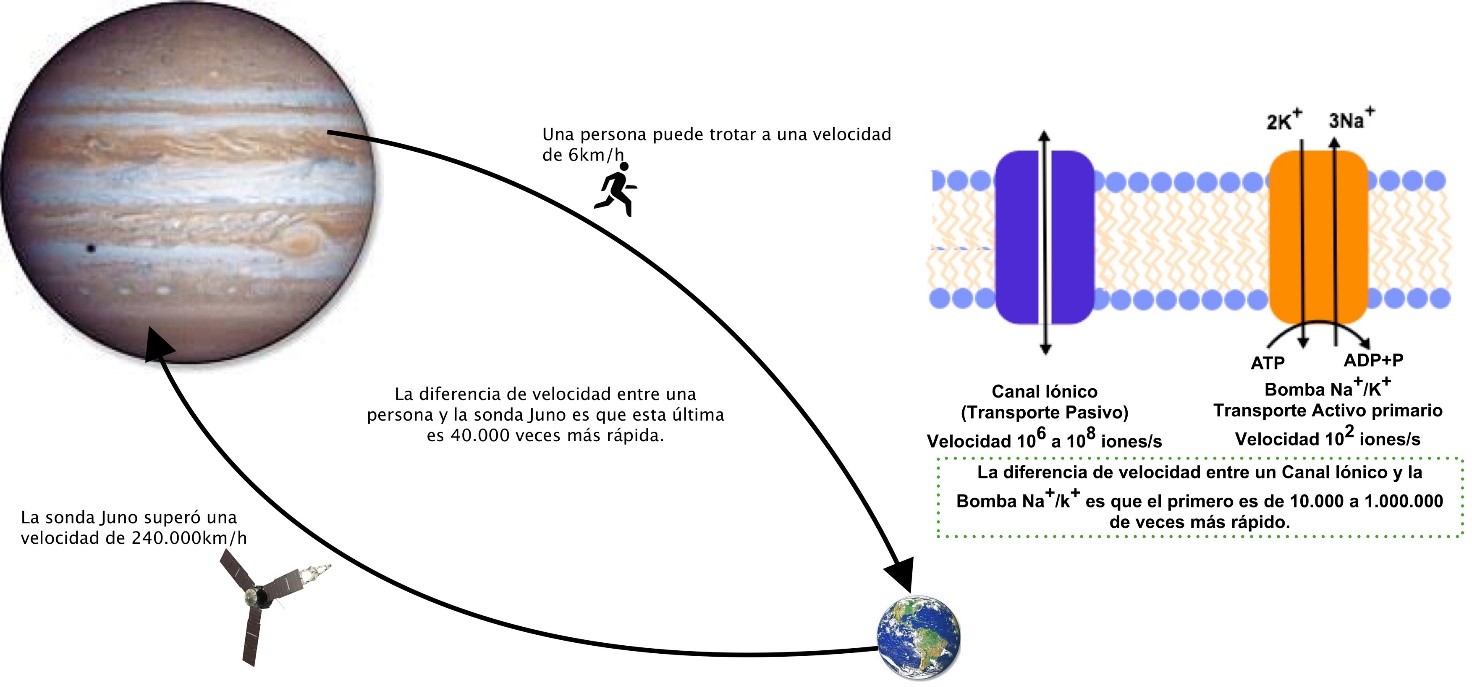
Figura 5: La diferencia de velocidad entre un canal iónico y la bomba Na+/K+, puede ser aún mayor que la diferencia de velocidad entre la sonda Juno y una persona que trota.
A modo de síntesis
Este artículo plantea una vieja problemática en la enseñanza del potencial de acción, constituida por la conceptualización errónea de que la bomba de sodio y potasio participa en la generación de potenciales de acción. Consideramos que el problema de fondo está en la omisión de una valoración cualitativa de “números” a los que solemos no prestar atención cuando enseñamos: ¿Cuánto cambia el valor de Vm durante un potencial de acción?, ¿el pasaje de cuánta carga, a través de las membranas celulares permite dicho cambio?, ¿con qué rapidez atraviesa las membranas esa carga eléctrica?, ¿cuánto valen las concentraciones iónicas en los medios intracelular y extracelular?, ¿cambian esas concentraciones por el pasaje de unos pocos iones?, ¿con qué rapidez pasan los iones a través de bombas?, ¿pueden las bombas “corregir” cambios en el Vm producidos por canales iónicos, en un intervalo de tiempo similar? Entendemos que en este caso, la omisión de datos numéricos y especialmente de su valoración cualitativa, es el origen de conceptos inclusores erróneos vinculados con cierta lógica que da coherencia a un aprendizaje que es significativo pero no sustentable del potencial de acción en neuronas. El Modelo de Aprendizaje Cognitivo Consciente Sustentable como marco teórico para analizar la problemática de enseñanza de estos temas nos permitió elegir conceptos sostén variados y abordar desde ellos una perspectiva didáctica para usar con docentes. Los conceptos sostén que permitieron valorar cualitativamente y comparar, determinados números que con frecuencia descuidamos en la enseñanza de la Biología fueron de impacto muy positivo y permitieron a los participantes de cursos una reflexión comprensiva del origen de sus propias concepciones errónas.
Notas al pie
1 Cabe destacar que el gradiente electroquímico no es sinónimo de gradiente químico. Es decir, cuando el soluto a considerar es un ión, no es correcto hacer deducciones sobre su tendencia al escape únicamente a partir de datos de su concentración, sino que dicha deducción podrá ser correcta únicamente al considerar el potencial de equilibrio electroquímico del ión calculado por la ley de Nernst.
2 Las respuestas eléctricas incluyen potenciales de acción y respuestas electrotónicas (también denominadas pasivas, graduadas, subumbrales). Ejemplos de estas últimas son: potenciales postsinápticos y potenciales receptor y generador.
3 Conductancia es la magnitud inversa a la resistencia. La unidad de resistencia es ohm, y de la conductancia mho.
4 Puede apreciarse cómo pequeños cambios eléctricos desde el punto de vista físico (cambios de potencial eléctrico en el orden de los milivoltios y de conductancias en el orden de los milimho), tienen relevancia biológica en tanto determinan “señales” que modifican respuestas fisiológicas.
5 La concentración de sodio extracelular es aproximadamente 145 mM, en tanto que la intracelular es cercana a 4mM. Las concentraciones de potasio en los medios intracelular y extracelular son de 140 mM y 4 mM, respectivamente.
Referencias:
1. Latorre R, López Barneo J, Bezanilla F, Llinás R (eds) (1996). Biofísica y fisiología celular. Sevilla: Universidad de Sevilla. Secretariado de Publicaciones.
2. Píriz Giménez, N (2016) Biofísica para la formación del Profesorado. Montevideo: Ediciones Ciencia. 2a edición.
3. Silverthorn, DU (2008) Fisiología humana. Un enfoque integrado. Buenos Aires: Editorial Médica Panamericana. 4a edición.
4. Cingolani, HE, Houssay, AB (2006) Fisiología humana. Buenos Aires: El Ateneo. 7ª edición.
5. Hille, B. (2001) Ion Channels of Excitable Membranes. Massachusetts: Sinauer Associates Inc. 3a edición
6. Skou, JC (1957) The influence of some cations on an adenosine triphosphatase from peripheral nerves. Biochimica et Biophysica Acta 23: 394–401
7. Píriz Giménez N, Añón JT, Balsas JL, Rattín E, & López MN (2016). Analysis and methodological approach to addressing the “myth of the sodium/potassium pump” when teaching the nerve impulse. International Educational Scientific Research Journal, 2(6): 104-106.
8. Galagovsky L (2004a). Del aprendizaje significativo al aprendizaje sustentable. Parte 1: el modelo teórico. Enseñanza de las Ciencias, 22(2): 229-240.
9. Galagovsky L (2004b) Del aprendizaje significativo al aprendizaje sustentable. Parte 2: derivaciones comunicacionales y didácticas. Enseñanza de las Ciencias, 22(3):349-364.
10. Píriz Giménez N, Terevinto Ziziunas E, Tucci Añón J, y Lezama Balsas J (2011) “NTICs en la Enseñanza de la Biología: una propuesta para el estudio del potencial de acción nervioso en formación terciaria y secundaria”. (En Saravay, M, Oroño, SU,Vieira, S. Actividades prácticas en la enseñanza de Biología para la formación de docentes: Una sistematización reflexiva. Disponible https://www.researchgate.net/profile/Silvia_Umpierrez_Orono3/publication/235970428_Actividades_practicas_en_la_ensenanza_de_la_Biologia_para_la_formacion_de_docentes_una_sistematizacion_reflexiva/links/02e7e51503a5a4427e000000.pdf
Webgrafía1. http://webspace.ship.edu/cgboer/genesp/potencial_accion.html (fecha de acceso: 1/8/18)
http://recursos.cnice.mec.es/biosfera/alumno/1bachillerato/animal/contenidos16.htm (fecha de acceso: 1/8/18)
2. http://www.hablemosdeneurociencia.com/conexion-neuronal-potencial-accion/ (fecha de acceso: 1/8/18)
3. https://prezi.com/wzjinhfgk3vg/bomba-sodio-potasio-y-potencial-de-accion/ (fecha de acceso: 1/8/18)
4. https://es.slideshare.net/lorenijiju/3-potenciales-de-membrana-y-potenciales-de-accin (fecha de acceso: 1/8/18)
5. https://www.youtube.com/watch?v=_FzAJMapHYE (fecha de acceso: 1/8/18)
6. https://www.youtube.com/watch?v=77wDRHpGay0 (fecha de acceso: 1/8/18)
7. https://www.youtube.com/watch?v=txGi8j5bvds (fecha de acceso: 1/8/18)
8. https://www.youtube.com/watch?v=fNrsxekCsnI (fecha de acceso: 1/8/18)
9. https://www.youtube.com/watch?v=KPAG_34Yh_o (fecha de acceso: 1/8/18)
|
Revista QuímicaViva Número 3, año 17, Diciembre 2018 quimicaviva@qb.fcen.uba.ar |