La Espectroscopía Infrarroja (FT-IR-ATR) como herramienta para identificar la degradación del polímero Polietilentereftalato - Bagazo de Caña
Márquez-Riquel María, Zara Joelmy
Laboratorio de Química Orgánica, Universidad Nacional Experimental Politécnica de la Fuerza Armada (UNEFA - Falcón)
Recibido: 22/03/2021 - Aceptado: 14/09/2021
Resumen
El presente trabajo dará a conocer como la espectroscopia infrarroja (FT-IR-ATR) es útil para determinar cuantitativamente la degradación del polímero Polietilentereftalato-bagazo de caña, utilizando las lecturas de los espectros infrarrojos en la determinación del índice de carbonilo (%IC), vinilo (C=C) y el porcentaje de reducción del índice carbonilo (%Red IC) y vinilo (%Red C=C), obteniéndose resultados entre el control (T0) y los tratamientos a 60 días de exposición fúngica de 100 a 51,20% en %IC, el %C=C paso a 61,77%,mientras 48,80% en %Red IC y 38,23% para %Red C=C. Finalmente se concluye que el uso de la herramienta para identificar y cuantificar la degradación del polímero es sencilla y confiable.
Palabras clave: Degradación del polímero; espectroscopia infrarroja, herramienta, índice carbonilo, índice vinilo.
Infrared Spectroscopy (FT-IR-ATR) as a tool to identify the degradation of polyethylenterfthalate polymer - Bagazo de Caña
Summary
The present work will show how the infrared spectroscopy (FT-IR-ATR) is useful to quantitatively determine the degradation of Polyethylenterefthalate polymer-bagazo de caña, using the readings of the infrared spectra in determining the carbonyl index (% CI), vinyl (C = C) and the percentage reduction of the carbonyl index (% Red IC) and vinyl (% Red C = C), obtaining results between the control (T0) and the treatments at 60 days of fungal exposure from 100 to 51.20% in% CI, while in% C = C it went to 61.77%, 48.80% in% Network IC and 38.23% for% Network C = C. Finally, it is concluded that the use of the tool to identify and quantify polymer degradation is simple and reliable.
Keywords: Polymer degradation; infrared spectroscopy, tool, carbonyl index, vinyl index.
Introducción
Los polímeros son compuestos orgánicos sintéticos derivados del petróleo y dependen en su totalidad de este recurso fósil no renovable, por lo que su degradación tarda muchos años aproximadamente entre 100 a 500 años al ser desechados en los vertederos de basura [1]. Uno de los polímeros más usados por su versatilidad, propiedades físicas, químicas, mecánicas y biológicas es el polietentereftalato (PET) ya que es muy difícil la degradación en el medio ambiente por microorganismos o procesos químicos como la oxidación [2]. La producción anual mundial para el 2020 se estima en más de 500 millones de toneladas, entre las principales industrias de consumo se encuentran las bebidas gaseosas, cosméticos por nombrar algunas que producen más de 500 mil millones de botellas de plástico de un solo uso cada año [3]. En Venezuela el consumo de plásticos está situado en torno a 65 Kg/habitante/año, lo que representa el 11% del total de la bolsa de basura, siendo el destino final de estos envases el basurero [4].
De esta forma, los materiales biodegradables se están haciendo cada vez una alternativa como sustituto de los polímeros sintéticos [5]. Sin embargo hoy en día, la combinación entre los polímeros sintéticos y los naturales ha sido un alternativa para la producción de polímeros biodegradables como es el caso del almidón termoplástico (TPS) por su bajo costo, abundancia de materia prima y facilidad de procesamiento [5]. Otra combinación es la mezcla del PoliEtilenTereftalato y el bagazo de caña de azúcar que le provee al material sintético la propiedad de ser degradado por los microorganismos (hongos, bacterias, levaduras, algas), siendo el bagazo de caña de azúcar un residuo rico en celulosa polímero natural que está constituido principalmente por glucosa, por lo que, el bagazo de caña de azúcar se ha empleado principalmente en la producción de papel [6]. No obstante se está incorporando el uso de este residuo agroindustrial en la producción de polímeros degradables siendo esta una alternativa para disminuir la contaminación por residuos sólidos.
La biodegradabilidad de los polímeros sintéticos se puede controlar mediante la incorporación de polímeros biodegradables del tipo éster [7], los cuales se diseñan con el objetivo de obtener una mayor degradación que la de los convencionales manteniendo las propiedades y funcionabilidad de un polímero convencional [1], entre estos polímeros se encuentra el Polietilentereftalato ya que presenta en su composición el grupo éster. Los procesos biológicos son los más efectivos y menos costosos, aunque no los más rápidos en solucionar el problema [8]. La biodegradabilidad describe el proceso de mineralización de las estructuras orgánicas por microorganismos [9], lo que favorece la incorporación de CO2 orgánico al ecosistema y no como fuente de gases invernaderos que se acumulan en la atmósfera.
Debido a que la biorremediación utiliza la capacidad enzimática de los organismos y microorganismos para degradar y transformar contaminantes [8]. Por su parte, los hongos son organismos que pueden presentarse en forma levaduriforme y filamentosa, capaces de producir enzimas intra y extracelulares, que tienen la capacidad de transformar cualquier tipo de sustrato orgánico [4]. Los hongos basidiomicetos, también conocidos como champiñones, se destacan por participar principalmente en el ciclo del carbono, una vez que son excelentes degradadores de la lignina y celulosa [10]. Uno de estos hongos es la especie Aspergillus, quien es un hongo ambiental capaz de transformar cualquier sustrato orgánico de forma inespecífica debido a la cantidad de enzimas que produce esta variedad de microorganismo. De este modo Acuña [11] cita en su trabajo a muchos autores “... que han demostrado que los hongos liberan proteínas hidrófobas que se ligan a la superficie del polímero produciendo mayor biomasa, sobreviviendo a condiciones de baja disponibilidad de nutrientes, bajo pH y humedad”.
En otro orden de ideas, la espectroscopia infrarroja con transformada de Fourier (FT-IR), es una técnica de análisis químico cualitativo que permite identificar los grupos funcionales de los compuestos orgánicos donde la muestra es sometida a irradiación infrarroja (longitud de onda 4000 – 400cm-1) con la herramienta de Reflectancia Total Atenuada (ATR) que permite analizar la muestra sin ser sometida a tratamientos previos para su análisis [12]. Por lo que favorece el análisis de las muestras ya que no se incorpora ninguna sustancia que pueda interferir en los resultados.
Para Araque [13], esta técnica puede ser utilizada para identificar compuestos orgánicos, polímeros, determinar composición de copolímero, determinar posibles vías de degradación de polímeros entre otras. Para esta investigación se trata de una técnica sencilla y de bajo costo por lo que el uso del FT-IR-ATR como herramienta para identificar la degradación del polímero y facilitar la cuantificación de la degradación o transformación de los grupos carbonilos presentes en el material a través del índice de carbonilo es objeto de este estudio [14–16]. Por lo que el presente estudio persigue como objetivo evaluar la espectroscopia infrarroja (FT-IR-ATR) para determinar cuantitativamente la degradación del polímero PoliEtilenTereftalato – Bagazo de caña mediante el análisis de los espectros obtenidos.
Materiales y Métodos
1. Toma de muestra después del proceso degradativo con hongos filamentosos ambientales como Aspergillus niger, Aspergillus fumigatus y Rhizopus spp. a partir de la micoteca LIADSA-UNEFM 2015.
2. Se realizo análisis FTIRATR a las muestras de PoliEtilenTereftalato sin tratar (T0), mezcla de polímeros (PET-Bagazo de caña) T0 y polímeros biotratados en el tiempo de 60 días (T60) con el objetivo de identificar las bandas y/o los grupos funcionales sensibles al ataque fúngico. Se utilizo un equipo Nicolet Is10 modelo Thermo Fisher Scientific, La toma de los datos se realizó con una escala de absorbancia desde 4000 hasta 600 cm-1 con 4 cm-1, con una resolución de 64 scans, y una ganancia de 8 y velocidad óptica de 0,4747. Utilizando el accesorio Thermo ITR ZnSe. Antes de las lecturas de las muestras se acondiciono el equipo tomando el aire como referencia antes de la recolección de cada espectro de la muestra (background).
Las muestras se colocaron directamente sobre el cristal de ZnSe. Cada muestra de las mezclas del polímero y su control fueron medidos por duplicado y colocados en la celda de ATR sin ninguna preparación ni dilución, se utilizó para procesar los espectros el programa OMNIC. Se analizaron las diferentes concentraciones del polímero.
3.- Se utilizo la metodología propuesta por Valea et al., [15] y Uribe et al., [16] modificada, en la determinación del porcentaje de índice de carbonilo (%IC) en función a la absorbancia del pico a 1713 cm-1 correspondiente al enlace carbonilo (C=O) presente en el PET sin tratamiento (control) y la mezcla PET-Bagazo de caña, con respecto a la absorbancia de la banda del enlace CH2 a 1455 cm-1 presente sin variación en el PET si tratamiento (control) y la mezcla PET-Bagazo de caña. Asimismo se siguió la metodología propuesta por Uribe et al., [16] modificada en la normalización de la zona C=C correspondiente a las longitudes de onda 1614, 1578 y 1504 cm-1, con la banda del enlace CH2 a la longitud de onda 1455 cm-1 que fue invariable para el polímero PoliEtilenTereftalato (control), Bagazo de caña y la mezcla PoliEtilenTereftalato -Bagazo de caña.
4.- Análisis estadístico de los datos se realizó mediante el uso del paquete estadístico Minitab 17® para Windows® realizando pruebas de homogeneidad seguido de un análisis de varianza con ajuste lineal por ANOVA y un post hoc de comparación múltiple de Tukey siendo la significancia del p- valor (p ≤ 0,05), expresadas en letras en las imágenes y tablas, donde letras iguales no hay diferencia significativa.
Resultados y Discusión
Se muestra el espectro infrarrojo separando dos zonas, una que va de 4000 a 1200 cm-1 que es la región de los grupos funcionales y otra que va de 1200 a 400 cm-1 que es la correspondiente a la huella digital, esta última es una zona invariante a menos que el compuesto haya sufrido algún efecto químico, físico o biológico [17]. En la figura 1 se observan las bandas vibracionales del PET en el infrarrojo medio donde se señalan las principales bandas a estudiar como son la del carbonilo presente en 1713 cm-1 [16,18], en 1455 cm-1 se presenta la banda del metileno [16,18,19] y otras regiones vibracionales características del compuesto que para la degradación en el presente estudio no se consideran.
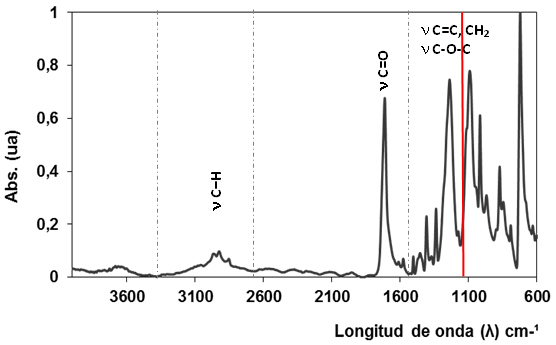
Figura 1:Espectro FT-IR-ATR del PolietilenTereftalato reciclado se muestran las zonas vibracionales C=O, C-O-C, -CH2, -CH, C=C [20].
En la figura 2 se muestran los espectros FT-IR-ATR del polímero sin tratar y biotratados en 60 días de exposición frente a especies fúngicas ambientales como son los hongos A. niger, A. fumigatus y Rhizopus spp. donde se observan las bandas vibraciones características para este estudio como son la región del carbonilo (C=O) a 1713 cm-1 [16,18] y la del metileno (CH2) en 1458 cm-1 y las bandas de los enlaces C=C Ar y C-CAr en 1614, 1578 y 1504 cm-1 respectivamente las cuales son representativas de los poliésteres [16,18,19], en la superposición de los espectros se puede ver como el tamaño de la banda del carbonilo se ve disminuida y/o aumentada en las mezclas A, B y C con respecto al control sin tratamiento fúngico.
Es de hacer notar que la banda del carbonilo es capaz de absorber energía lumínica que permite que estos materiales sean fotodegradable [1], lo que permite la acción de los microorganismos en la degradación del material, otro factor que coadyuva a la transformación son las características del polímero como: la presencia de enlace susceptibles a hidrólisis, hidrofilicidad, estereoquímica, peso molecular, superficie especifica, entre otras [1]. Por todo esto se puede inferir que el polímero PoliEtilenTereftalato -Bagazo de caña de azúcar sufrió transformación o degradación frente a las especies fúngicas utilizadas, así como también el efecto fotodegradante que pudo contribuir al proceso de conversión.
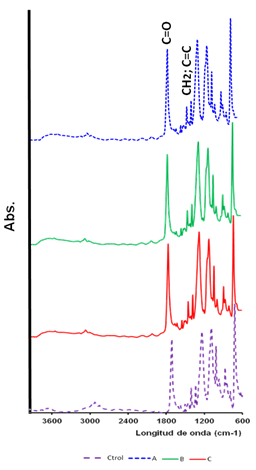
Figura 2:Espectro FT-IR-ATR del polímero PoliEtilenTereftalato T0 y los Biotratados T60, se muestran las bandas vibracionales correspondientes a los grupos funcionales presentes en los materiales C=O, C=C, CH2.
En la tabla I se observan los resultados obtenidos de los análisis espectrales de los infrarrojos, donde se aprecia lo siguiente en función al control PoliEtilenTereftalato-Bagazo de caña T0 y los tratamientos con las especies fúngicas a los 60 días de exposición. Ahora bien a través de la herramienta del FT-IR-ATR se puede evaluar o demostrar la degradación o transformación por acción de algún agente sobre los materiales complejos sintéticos en función al índice de carbonilo y metileno [16], ya que un aumento o disminución de estos grupos funcionales es indicativo de los cambios de los compuestos orgánicos mediante la acción de un organismo vivo.
Se pueden observar cuatro grupos estadísticamente significativos (p≥0,05) entre las mezclas en el tiempo, y el control formando este el grupo (b), de igual forma se percibe que las tres especies (A. fumigatus, A. niger y Rhizopus spp.) forman el grupo (a) quienes logran disminuir el índice carbonilo (%IC) desde 90,83 a 51,20% y el porcentaje de vinilo (%C=C) que disminuyo desde 97,97a 61,77 % con respecto al control que presenta 100%. Por lo que Uribe et al., [16] y Aradilla-Zapata et al., [1], afirman que durante el proceso de degradación, el grupo funcional carbonilo es liberado por acción de la luz UV y rápidamente asimilado como fuente de energía por los microorganismos, que a su vez podría permitir la mayor degradación de la estructura principal de la molécula en este caso del PoliEtilenTereftalato-Bagazo de Caña.
Del mismo modo se observa la formación de dos grupos (c,d) entre Red %IC y Red %C=C donde los valores oscilan entre 48,80 y 2,03% respectivamente, por esta razón la reducción del índice carbonilo guarda relación con la disminución del índice de terminaciones vinílicas (C=C), siendo otro factor importante el tipo y características de los microorganismos empleados para el estudio [1,16] por lo que se demuestra que la técnica de FT-IR-ATR se puede emplear para la cuantificación de la degradación microbiana de los materiales complejos (polímeros).
Tabla I: Evaluación del polímero PoliEtilenTereftalato-Bagazo de caña en función al Índice de carbonilo y reducción del %C=C después del biotratamiento con las especies fúngicas A. fumigatus, A. niger y Rhizopus spp. y sus controles. Se muestran el promedio n=3, la desviación estándar y la significancia del p-valor en letras iguales entre columnas no hay diferencia significativa (p≤0,05). Fuente: Espectros infrarrojos de cada especie, mezcla A: 95:5; B: 90:10, C: 85:15 control T0 y biotratamientos a T60.
| Especies | Mezclas/Tiempo (días) (b) | %IC (a) | Red %IC (c) | %C=C (a) | Red %C=C (d) |
|---|---|---|---|---|---|
| Control (b) | A- T0 B- T0 C- T0 | 100 100 100 | --- --- --- | 100 100 100 | --- --- --- |
| A. fumigates (a) | A- T60 B- T60 C- T60 | 82,36±7,82 90,83±3,61 86,84±13,89 | 17,64 10,45 13,16 | 95,96±0,35 77,69±0,38 81,38±0,10 | 4,04 22,31 18,62 |
| A. niger (a) | A- T60 B- T60 C- T60 | 61,83±8,19 86,87±12,32 51,20±8,42 | 38,17 13,13 48,80 | 97,97±0,38 84,04±3,30 82,64±1,22 | 2,03 15,96 17,36 |
| Rhizopus spp. (a) | A- T60 B- T60 C- T60 | 80,85±13,37 70,95±4,76 87,57±9,91 | 19,15 29,05 12,43 | 97,35±0,82 79,27±0,36 61,77±0,53 | 2,65 20,73 38,23 |
Conclusiones
La identificación de los grupos funcionales en el espectro infrarrojo del polímero PoliEtilenTereftalato – Bagazo de caña susceptibles a degradación se logro satisfactoriamente ubicando los grupos carbonilo (C=O), metileno (CH2) y la vibración del enlace C=C, en el PoliEtilenTereftalato y los polímeros PoliEtilenTereftalato-Bagazo de caña de azúcar control y biotratados en las mezclas estudiadas, identificándose las bandas sin cambios en los polímeros estudiados.
La Cuantificación de la degradación del polímero PoliEtilenTereftalato – Bagazo de caña por espectroscopia infrarroja con transformada de Fourier (FT-IR-ATR) se alcanzo a través del %IC y Reducción del %IC, %C=C y la Reducción %C=C por lo que el uso de esta herramienta es sencilla y confiable para demostrar la degradación o transformación del polímero PoliEtilenTereftalato – Bagazo de caña.
Agradecimientos
Los autores agradecen el apoyo a la investigación a la Licda. Liz Cubillan del Instituto Venezolano de Investigaciones Científicas (IVIC) de la unidad de servicios de infrarrojo centro de química (PAS), y a la Ing. Patricia Navas del Laboratorio de Investigación y Apoyo Docente Santa Ana (LIADSA-UNEFM).
Referencias:
[1] Aradilla Zapata D, Oliver R, and Estrany F. (2012) Polímeros biodegradables : una alternativa de futuro a la sostenibilidad del medio ambiente. Técnica Ind. marzo: 76–80.
[2] Muñoz L. (2012) Estudio del uso del polietilen tereftalato (PET) como material de restauracion en suelos de baja capacidad de carga. Accesado en: 2018.
[4] Márquez-Riquel M, Salazar-Cordero J, Yegres F, Nuñez Y, and Navas P. (2016) Degradacion parcial del copolimero polipropileno de alta densidad y bagazo agave cocuy mediada por hongos filamentosos. Agora Cient. UNEFM 740–746.
[5] Mendoza Quiroga R, and Díaz Velilla W. (2011) Metodología para la caracterización termo-mecánica de películas plásticas biodegradables Methodology for the thermo-mechanical characterization. Prospectiva 9: 46–51.
[6] Zara J, Yegres F, Vargas N, Morales S, Cubillan L, and Márquez-Riquel M. (2017) Empleo de la Espectroscopia Infrarroja ( FT-IR-ATR ) como herramienta para la Caracterización del bagazo de caña proveniente de la Sierra Falconiana. QuimicaViva 16: 17–24.Accesado en: 2011.
[8] Márquez-Riquel M, Navas-Yamarte P, Yegres F, and Vivas-Espejo C. (2015) Biodegradación parcial de aceites residuales usados utilizando Aspergillus niger, Rhizopus sp. y Saccharomyces cerevisiae. Rev. QuímicaViva 14: 90–102.
[9] Rodríguez A. (2012) Ecnología de Alimentos Biodegradabilidad. Cienc. y Tecnol. Aliment. 22: 69–72.
[10] Ferri GN, Hermann KL, Wisbeck E, and Tavares LBB. (2014) Evaluación de la influencia de los factores físicos y nutricionales para la propagación del micelio de Pleurotus sajor-caju CCB-019 en biomasa. .
[11] Acuña N. (2017) Revisión bibliografíca sobre los microorganismos Biodegradadores de Polietileno de Baja densidad y sus efectos en el material. .
[12] Ramirez A, Benítez JL, Rojas de-Astudillo L, and Rojas B. (2016) Materiales Polímeros de tipo Hidrogeles: Revisión sobre su caracterización mediante FTIR, DSC, MEB y MET. Rev. Lat. Met. Mat. 36: 108–130.
[13] Araque Nohemi. (2008) Estudio y caracterizacion de la degradacion hidrolitica y en compostaje de PET virgen y reciclado.
[14] Gallego K, López B, and Gartner C. (2006) Estudio de mezclas de polímeros reciclados para el mejoramiento de sus propiedades. Rev. Fac. Ing. Julio: 59–70.
[15] Valea A, Juanes F, Miguez J, and Gonzales M. (2008) Aleaciones de polipropileno (PP) y Polietilentereftalato (PET) reciclados y estudio de sus propiedades. An. Mecánica la Fract. 2: 5.
[16] Uribe D, Giraldo D, Gutierrez S, and Merino F. (2010) Biodegradación de polietileno de baja densidad por acción de un consorcio microbiano aislado de un relleno sanitario. Rev Perú Biol 17: 133–136.
[17] Gulmine J.V., P.R. Janissek, H.M. Heise et al. (2002) Polyethylene characterization by FTIR. Polym. Test. 557–563.
[18] Palma D. (2012) Producción de polímeros biodegradables mediante la modificación del PET con APL y Quitosano. .
[19] San Andres M, Gomez M, and De la Roja J. (2009) Materiales sintéticos utilizados en la manipulación, exposición y almacena-miento de obras de arte y bienes culturales. Caracterización por espectroscopia FTIR-ATR. .
[20] Márquez-Riquel M, Zara J, Cordoba Y, and Cubillan L. (2019) Copolymer got from PET-BC as a technological alternative in the reuse a solid waste. IJLEMR 4: 51–57.
|
Revista QuímicaViva Número 3, año 20, Diciembre 2021 quimicaviva@qb.fcen.uba.ar |